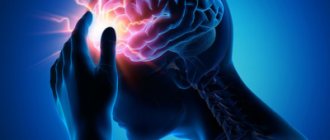
Фонетограмма больной 18 лет. Студентка вокального отделения музыкального училища. Сопрано. Диагноз: парез левой голосовой складки после острого респираторного заболевания. Срок болезни — 4 нед. а — значительное сужение частотного диапазона (менее 1 октавы, 136,51 Гц) и смещение его в сторону низких частот. Сужение динамического диапазона (18,5 дБ), укорочение ВМФ (11,74 с); б — через 1,5 мес после проведения электростимуляции гортани и приема нейромидина. Расширение вокального профиля за счет нарастания частотного (369,02 Гц) и динамического (38,0 дБ) диапазонов голоса. ВМФ — 17,9 с.
Односторонний парез голосовых складок (ОПГС) относится к органическим заболеваниям гортани, при которых ограничены или полностью отсутствуют движения голосовой складки на стороне поражения вследствие расстройства иннервации мышечного аппарата органа, что затрудняет или делает невозможным регулирование голосовой функции. Считается, что диагноз «парез» гортани правомочно выставлять при длительности заболевания не более года, в противном случае более правильным является диагноз «паралич» [1, 2].
Ведущими причинами ОПГС являются опухолевые процессы и хирургические вмешательства на различных органах шеи и грудной клетки, чаще всего на щитовидной железе [3—5]. Однако примерно в 14% случаев заболевание может протекать бессимптомно, т. е. без расстройства голосовой и дыхательной функции гортани [6]. Интересно, что операции, проведенные на щитовидной железе, даже в условиях идентификации возвратного нерва, не исключают возникновения пареза голосовых складок. Согласно данным Т.В. Готовяхиной [7], частота ОПГС при первичных хирургических вмешательствах на щитовидной железе составляет 7,5%. Проведение консервативного лечения с первых суток заболевания обеспечивает восстановление подвижности голосовых складок в 87,5% случаев. Причем на реабилитацию таких пациентов требуется в среднем не менее 2 мес. В случаях отсроченной терапии хотя бы на 1 мес эффективность снижается до 55,5%, на 2—3 мес — до 32,7%, на 4—6 мес — до 12,2%. При длительности пареза более 6 мес восстановления функции гортани, как правило, не происходит [7].
Диагностика расстройства подвижности голосовых складок при парезе, как правило, не представляет трудностей. В большинстве случаев с этой целью применяется ларингостробоскопия. Лишь 1,7% оториноларингологов в своей практике пользуются электромиографией, которая считается наиболее информативным методом в дифференциальной диагностике между парезом и параличом гортани [8].
ОПГС значительно снижает качество жизни пациентов и нередко создает угрозу профессиональной пригодности. Поэтому разработка новых методик консервативного и хирургического лечения заболевания по-прежнему остается актуальной. Одним из последних достижений в данном направлении являются работы, посвященные хирургической реиннервации вокальной мышцы гортани методом имплантации нервно-мышечного лоскута на ножке через окно щитовидного хряща и смещения черпаловидного хряща медиально. Подобные операции позволяют восстановить тонус и вибрацию голосовой складки на стороне пареза с хорошим результатом. Однако данный подход не применим в раннем периоде болезни, а рекомендуется лишь по истечении 6 мес безуспешного консервативного лечения [9]. В связи с этим значительная роль в реабилитации голосовой и дыхательной функции гортани при ОПГС отводится стимулирующей терапии, которая состоит в активации регенеративных процессов, перекрестной и остаточной иннервации мышц гортани и компенсаторных механизмов, позволяющих достичь наиболее полного смыкания голосовых складок при фонации, а также в предотвращении атрофии мышечного аппарата гортани.
Цель нашего исследования — оптимизация консервативного лечения больных с ОПГС.
Пациенты и методы
Исследование проводилось на клинической базе кафедры оториноларингологии ГБОУ ВПО ЯГМУ и в ООО «Медицинский Центр Авиценна», Ярославль. Обследованы 50 пациентов с парезом гортани: 45 женщин и 5 мужчин от 18 до 70 лет. Критерии включения в исследование:
возраст старше 18 лет, одностороннее нарушение подвижности гортани, срок заболевания не более 6 мес.
Критерии исключения:
наличие противопоказаний для электростимуляции гортани и назначения холинергического препарата нейромидин (ипидакрин, АО «Олайнфарм»), которые составили основу комплексной терапии больных с ОПГС. Таковыми критериями стали: индивидуальная непереносимость препарата, язвенная болезнь желудка и двенадцатиперстной кишки, тяжелая патология печени и почек, обострение течения бронхиальной астмы, стенокардия, брадикардия, механическая непроходимость желудочно-кишечного тракта и мочевыводящих путей, наличие эпизодов судорожного синдрома, кардиологических или других имплантированных электростимуляторов, металлических протезов в области шеи и головы, злокачественных новообразований любой локализации, предшествующее в течение 5 лет хирургическое вмешательство, выполненное по поводу рака щитовидной железы, поражение участков кожи, которые в процессе электростимуляции мышц гортани будут подвергаться воздействию, беременность и период лактации.
Ведущим этиологическим фактором развития ОПГС была операция на щитовидной железе, выполненная по поводу различной патологии: диффузный зоб, узловой зоб, аутоиммунный тиреоидит. Таких пациентов было 39 (78%). Объем хирургического вмешательства был различен: от частичной резекции — тиреоидотомии до полного удаления органа — тиреоидэктомии. У 5 (10%) пациентов ОПГС развился вследствие вирусной инфекции. В 6 (12%) случаях причину заболевания установить не удалось, поэтому процесс рассматривался как идиопатический. Средняя продолжительность болезни составила 1,9±0,7 мес. Самое раннее обращение за специализированной медицинской помощью было через 3 недели с момента развития ОПГС, самое позднее — через 5 мес 12 дней.
Степень поражения иннервации мышечного аппарата гортани определяли при помощи аппарата vocaSTIM-Master («Физиомед», Германия), который позволяет оценить так называемый коэффициент аккомодации (α), представляющий собой соотношение двух пороговых величин: гальванического порога тетанического сокращения мышц гортани под воздействием треугольных токов к реобазе, полученной при действии токов прямоугольной формы. В норме α находится в пределах от 3 до 6. Значение ниже 3 свидетельствует о снижении аккомодационной способности мышц гортани и начале их денервации (парез). Коэффициент α от 1 и ниже означает полную потерю аккомодационной способности мышц гортани, что указывает на наличие паралича. В исследование включали пациентов с уровнем α выше 1.
Путем случайной рандомизации пациенты были объединены в две группы, А и Б по 25 человек в каждой. Группы были статистически сопоставимы по возрастным и половым признакам, этиологическим факторам, клиническим и функциональным характеристикам, а также по длительности течения заболевания (Levene Test: р
>0,05). В обеих группах использовалось комплексное лечение, включающее дыхательную гимнастику, тренинг наружных мышц шеи, витаминотерапию, нейромышечную электрофонопедическую стимуляцию (НМЭФС) гортани и стандартные голосовые упражнения, которые пациент после предварительного обучения ежедневно выполнял в домашних условиях.
В группе, А лечение дополнялось назначением холинергического препарата нейромидин, который оказывает стимулирующее влияние на проведение импульса по нервным волокнам, межнейрональным и нервно-мышечным синапсам центральной и периферической нервной системы. Фармакологическое действие препарата основано на сочетании двух механизмов действия: блокады калиевых каналов мембраны нейронов и мышечных клеток и обратимого ингибирования холинэстеразы в синапсах, за счет чего нейромидин не только улучшает проведение импульса в нервной системе, но и усиливает сократимость гладкой мускулатуры. Кроме того, нейромидин обладает ноотропным, мнемотропным и психостимулирующим действием. Последнее достаточно важно для пациентов, страдающих парезами гортани, так как потеря звучности голоса в значительной степени сказывается на качестве их жизни. Согласно современным доказательным исследованиям, нейромидин активирует адаптивную нейропластичность [10], что ускоряет процессы восстановления поражений нервной системы различной локализации. Нейромидин активирует процессы восстановления как в центральной, так и в периферической нервной системе — это его принципиальное отличие от других антихолинэстеразных препаратов. Данное свойство препарата позволяет сохранять активность проекционных зон в центральной нервной системе при поражении периферической иннервации, что повышает эффективность терапии. Нейромидинназначали в течение первых 10 дней в виде внутримышечных инъекций по 15 мг 1 раз в день, затем переходили на пероральный прием в дозировке по 1 таблетке (20 мг) 3 раза в день. Общий курс лечения составил 45 дней. У пациентов группы Б нейромидинне использовался.
Электростимуляция гортани в обеих группах осуществлялась при помощи прибора vocaSTIM-Master, работающего в режимах импульсных токов низкой и средней частоты. Подача токов к мышцам гортани проводилась с помощью ручного ключа самим пациентом. Методика лечения представляет собой комбинацию сокращений мышц гортани под воздействием импульсных токов в ответ на одновременное выполнение больным фонопедических упражнений, которые подбирались для каждого пациента индивидуально по коэффициенту α. Курс НМЭФС состоял из 40 сеансов по 2 сеанса в день в течение 20 дней. По истечении этого периода пациенты выполняли комплекс фонопедических упражнений самостоятельно.
Оценка результатов терапии производилась через 45 дней. Восстановление подвижности голосовой складки в полном объеме оценивалось как «выздоровление». Восстановление звучности голоса при сохранении визуальной картины пареза характеризовалось как «улучшение». Сохранение неподвижности голосовой складки и дисфонии на прежнем уровне признавали как «отсутствие эффекта». Критериями анализа были избраны методики, принятые в качестве стандартов в современной оториноларингологии и фониатрии и позволяющие оценить клиническое и функциональное состояние гортани. Для определения подвижности голосовых складок, их вибраторной активности, степени смыкания при фонации использовалась оптическая ларингостробоскопия. Динамика дыхательной функции гортани изучалась методом скрининговой флоуметрии при помощи портативного флоуметра ATS 97 с фиксацией объема форсированного вдоха (ОФВ) в л/мин. Голосовая функция гортани исследовалась с применением шкалы GRBAS при субъективном прослушивании голоса пациента тремя независимыми экспертами и акустического анализа голоса.
Оценка голоса по шкале GRBAS осуществлялась по пяти стандартным признакам: «grade» (G) — выраженность дисфонии, «roughness» ® — грубость, резкость голоса, «breathiness» (B) — расстройство дыхания, наличие одышки, придыхания, «asthemicity» (A) — слабость голоса, «strain» (S) — напряжение голоса. Каждый критерий определялся в баллах от 0 до 3, где 0 — норма, 1 — слабая выраженность симптома, 2 — умеренное проявление, 3 — сильно выраженный симптом. Акустический анализ проводили с помощью компьютерного программного обеспечения «The lingWAVES Phonetogram Pro» («ATMOS», Германия) с записью фонетограммы. При этом оценке подлежали следующие показатели: время максимальной фонации (ВМФ), нестабильность (пертурбация) основного тона (Jitter), частотный и динамический диапазоны, интенсивность громкого голоса, индекс дисфонии (Dysphonia Severity Index, DSI). Кроме того, у больных произведена оценка качества жизни. С этой целью использовался специализированный опросник Voice Handicap Index (VHI) в его полной версии. Все исследования проводились дважды: до начала лечения и по истечении 45 дней терапии.
Статистический анализ полученных данных осуществлялся с помощью программ Statistica версия 10. При сравнении групп, А и Б достоверными считались различия, если полученное значение p
для сравниваемого критерия было ниже критического уровня значимости α=0,05. Сравниваемые признаки классифицировались как количественные. Для их оценки и проверки статистических гипотез использовались анализ соответствия вида распределения значений признака закону нормального распределения с помощью критерия Шапиро—Уилка, описательная статистика, двусторонний тест для независимых переменных, тест Левена на однородность дисперсий и параметрический анализ вариаций.
КЛАССИФИКАЦИЯ
Существует несколько форм дисфонии, которые зависят от характерных особенностей.
| Мутационная | Данная форма свойственна подросткам мужского пола, начинает “ломаться” голос. Увеличивается кадык, повышается количество слизи и появляется отечность. |
| Спастическая | Нет вибраций в голосовых связках. Происходит это по причине импульсивных сокращений внутренних мышц гортани. Поэтому ребенку так сложно говорить. |
| Психогенная | Отсутствует звучность голоса, но малыш способен говорить шепотом. Зачастую такая форма преобразуется в афонию. |
| Функциональная | Нарушения голосовых функций, характерно неполное смыкание голосовых связок. Но при этом исключены патологические изменения в области гортани. |
Для того, чтобы исправление дисфонии у ребенка проходило быстрее, необходимо определить форму заболевания.
Результаты и обсуждение
Основными жалобами больных до начала терапии были расстройство тембра голоса в виде охриплости, усиливающейся после голосовой нагрузки (90% наблюдений) либо афонии (10%), покашливание (100%), одышка при разговоре (72%) и/или при физической нагрузке (94%), поперхивание во время приема жидкой или твердой пищи (34%). Выраженность симптомов определялась ограничением подвижности и вибраторной активности голосовой складки на стороне поражения (3 пациента в группе, А и 4 пациента в группе Б) либо полной неподвижностью складки при фонации (22 и 21 пациент соответственно), что подтверждалось данными стробоскопии. В большинстве случаев (90%) голосовая складка на стороне поражения находилась в парамедианном положении (22 наблюдения в группе, А и 23 — в группе Б). Лишь у 10% больных (3 из группы, А и двое из группы Б) имелось латеральное расположение складки, что явилось причиной афонии, создавало дополнительные трудности в терапии и ухудшало прогноз заболевания.
В ходе исследования доказано, что добавление в схему терапии ОПГС холинергического препарата нейромидин позволяет достичь лучших результатов. Так, в группе, А выздоровление наступило у 5 больных (20%), улучшение — у 17 (68%), без эффекта было 3 случая (12%). В группе Б выздоровление имело место только у 2 пациентов (8%), улучшение — у 16 (64%), отсутствие эффекта — у 7 (28%). Таким образом, общая результативность комплексного лечения пациентов группы, А составила 88%, в группе Б —72%. Различия между группами статистически достоверны по двум оценочным параметрам: «выздоровление» и «без эффекта» (р
<0,05).
Представленные выше данные были подтверждены на основании анализа динамики сравниваемых параметров состояния дыхательной функции гортани, голоса и качества жизни пациентов. Отмечено, что ОФВ до лечения был значительно снижен в обеих группах: в группе, А — 147,2±32,0 л/мин, в группе Б — 152,6±37,9 л/мин. В процессе лечения отмечалась положительная динамика показателя, но в группе, А ОФВ вырос до 288,7±37,7 л/мин, т. е. практически в 2 раза, а в группе Б прирост ОФВ в среднем не превысил 45 л/мин и составил 197,2±34,5 л/мин. Различия между группами статистически достоверны, р
<0,05.
До лечения показатель GRBAS составил 8,4±1,2 балла в группе, А и 8,3±1,7 балла в группе Б, после лечения — 4,1±0,6 и 5,9±0,7 баллов соответственно (р
<0,05). Установлено, что в группе, А по сравнению с группой Б отмечалась более выраженная динамика практически всех акустических параметров голоса. Так, первоначальное значение ВМФ в группе, А составило 5,2±1,4 с, после лечения — 11,6±1,7 с. В группе Б ВМФ увеличилось с 6,0±1,6 с до 9,1±0,6 с. В группе, А отмечалось расширение частотного диапазона вдвое, с 128,1±37,3 Гц до 275,3±46,7 Гц, динамического диапазона — с 14,0±2,3 дБ до 24,0±2,7 дБ (
р
<0,05). В группе Б динамика показателей была не столь заметной. Частотный диапазон увеличился с 139,0±26,3 Гц до 195,3±22,6 Гц, динамический диапазон — с 14,9±1,9 дБ до 19,0±1,3 дБ. В группе, А показатель нестабильности голоса по частоте уменьшился втрое, с 3,4±1,5% до 1,0±0,3%. В группе Б Jitter оставался достаточно высоким, с 3,2±1,8% снизился лишь до 2,9±0,3%, что объясняло сохранение тремоляции и диплофонии в голосе пациентов. Изменение представленных выше акустических параметров сопровождалось смещением индекса дисфонии в сторону положительных значений. Однако в группе Б эти изменения были не столь заметными (от –2,9±2,3 до –0,1±1,4) по сравнению с группой, А (–3,0±1,7 до –1,9±2,3). Различия между группами статистически достоверны,
р
<0,05.
Тем не менее следует отметить, что по ряду параметров существенных различий между группами не установлено. Так, у пациентов группы, А сила громкого голоса выросла с 74,0±4,5 дБ до 85,8±6,9 дБ, в группе Б — с 75,8±6,6 дБ до 84,7±5,5 дБ (р
>0,05). При этом средние значения показателя были вполне удовлетворительными в обеих группах и соответствовали возрастной норме. Динамика показателя качества жизни также не имела достоверных различий между группами. В группе A VHI до лечения составил 84,9±12,6 балла, после лечения — 27,0±9,6 балла. В группе Б VHI уменьшился с 81,0±20,2 до 32,1±11,7 балла (
р
>0,05). В целом в обеих сравниваемых группах VHI не соответствовал нормальным значениям, что свидетельствовало о сохранении расстройства качества жизни у большинства пациентов.
На рисунках
представлены фонетограммы пациентки из группы А. Динамика вокального профиля наглядно демонстрирует эффективность комплексного лечения ОПГС. В данном наблюдении достигнуто полное восстановление подвижности голосовой складки на стороне поражения.
Анализ всех случаев неэффективности проводимой терапии, а также неудовлетворенности пациентов в отношении динамики голосовой функции позволил предположить, что возможными причинами отсутствия эффекта являются позднее обращение пациентов за медицинской помощью (по истечении 2 мес и более), латеральное расположение голосовой складки на стороне поражения, а также неисполнение пациентом рекомендаций о целесообразности систематического выполнения фонопедических упражнений.
Необходимо отметить, что большинство пациентов группы, А удовлетворительно переносили прием нейромидина, несмотря на длительный курс терапии. Побочные эффекты и нежелательные явления зафиксированы только в 2 (8%) случаях из 25. Одна пациентка, женщина 67 лет, пожаловалась на слабость и тремор рук после перехода с инъекционной формы нейромидина на таблетированную. Симптомы исчезли через сутки без отмены препарата. Вторая больная, женщина 46 лет, отмечала частые головные боли в течение всего периода терапии нейромидином. В данном случае отмены препарата также не потребовалось.
Как работает наш голосовой аппарат?
Прежде чем разбираться с причинами, из-за которых пропадает или садится голос, нужно понять, как работает наш голосовой аппарат. Воздух, выходя из лёгких на выдохе, встречает на своём пути определённые препятствия, сталкивается с ними, тем самым приводя к возникновению звуковых колебаний. Если бы воздуху ничего не мешало, звуки бы не образовывались, а значит и говорить мы бы не могли.
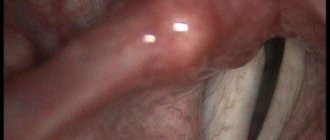
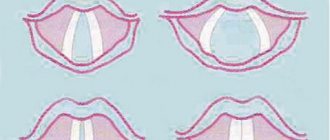
Таким естественным препятствием для воздушного потока служит гортань, а точнее расположенные на ней голосовые связки. Голосовые связки представляют собой складки на слизистой оболочке гортани. Между ними расположена щель. Когда человек молчит, щель широко раскрыта. Во время разговора или пения она сужается. Проходящий через связки воздух заставляет их быстро колебаться и вибрировать. Именно так возникает звуковая волна, и зарождается голос. Вполне логично, что, если пропадает или садится голос, значит проблема связана с голосовыми связками и сбоем в работе голосового аппарата.
Выводы
Парез гортани — частое осложнение, возникающее после различных заболеваний и оперативных вмешательств. ОПГС характеризуется значительными нарушениями всех акустических характеристик голоса, что, безусловно, влияет на качество жизни больных и их коммуникативные способности.
Полученные в ходе проведенного исследования данные свидетельствуют о целесообразности проведения при ОПГС комплексной терапии, представляющей сочетание электростимуляции гортани, фонопедии и назначения холинергических препаратов. Добавление нейромидина в общепринятую схему консервативного лечения позволяет повысить его результативность с 72 до 88%.
В заключении следует подчеркнуть, что в случаях развития ОПГС необходимо корректное отношение к пациенту, приложение максимума усилий, настойчивости и профессионализма для восстановления функции гортани или, по крайней мере, улучшения качества голоса.